產品課堂
APC相襯技術在細胞顯微成像中運用的技術原理及啟示——上
自Frits Zernike發明相襯顯微觀察技術以來,基于惠更斯—菲涅耳原理用函數方法驗證和推導其成像機制的研究繁多,但以問題為導向,從微觀視角探究困擾細胞相差成像中的偽影等圖像亮度分布失衡現象產生的必然性并提出系統性解決方案的,則少之又少。這種現狀的存在,分析起來可能是這個幾個因素造成的。
一是硬件上,相襯技術幾乎離不開相差物鏡,而相差物鏡難免會降低熒光成像質量。改進相差圖像品質的努力前景不佳。二橫向對比看,同樣是采用透射光光路,用DIC、霍夫曼觀察法所獲得的圖像,無論是圖像對比度、細胞內部結構細節表現力均優于相差法,且厚薄樣品通吃,明場物鏡、熒光物鏡均適用,足以替代相差技術。第三是科研考評價值上,經典技術方法體系的二次開發與再認識的技術前瞻性、研究成果學術影響力可能不夠。這種顧慮影響了人們以此選題攻關的積極性。所以,盡管發現相差圖像偽影問題由來已久,但探索解決問題的實踐和成果產出屈指可數。
早在2005年,Leica將新型內置相襯技術(Intermediate Phase Contrast, IPH) 引入到DMI3000B倒置顯微鏡上。IPH是將相差物鏡內置相位板移出,做成與環形光闌滑塊類似的獨立相襯模塊(Phase Contrast module),在物鏡與目鏡間傳輸光路的中間出瞳界面(Intermediate pupil interface)設置前置模塊(Front Module)作為相位板滑塊安裝插槽,達到了對透射光相襯調制目的,且便于根據觀察需要即插即拔。最關鍵的是,IPH方法實現了物鏡與相位板的分離,配置普通平場熒光物鏡不僅獲得對比度極佳的相差圖像,更契合對高品質熒光成像的需求。
雖然IPH相襯技術解決了相差物鏡對熒光圖像質量潛在影響問題,但圖像偽影困擾問題依舊。
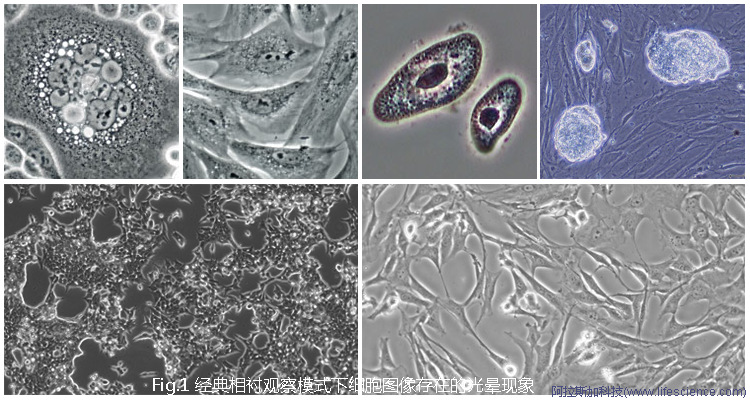
傳統相差顯微鏡采集的細胞相差圖像中最常見的偽影效應是光暈,是指圍繞在細胞與細胞器外緣亮度極高的光環。它掩蓋細胞邊緣輪廓和細胞內部結構細節,干擾對鏡下細胞形態和細胞功能狀態的觀察與分析。
在經典相襯技術誕生前,人們迫切需要找到一種能將透明相位體看起來更暗的技術方法。而有加工質量缺陷的衍射光柵的衍射光譜中所出現的黑色羅蘭鬼線(Rowland ghosts),激發了科學家將細胞與光柵表明的瑕疵位點聯系起來,用光波干涉產生暗條紋的原理讓細胞原形畢露的靈感。當然,細胞比機器加工失誤所致光柵局部外形要復雜得多。透射光與細胞樣品相互作用時,產生直射光、折射光、衍射光及雜散光。鏡下的細胞圖像是多種光波相互疊加的綜合結果,非光波干涉單一機制所決定。
迄今為止,對光暈的產生機制可能有多種解釋。如折射率不同晶體間接觸界面的貝克線理論(限于篇幅在此不作討論)、衍射與直射光竄擾污染原理及角度依賴性圓孔衍射原理等。
一、細胞相差成像中的光竄擾污染
早在Frits Zernike創建相襯顯微技術的過程中就已發現,如直射光亮度遠高于衍射光,則鏡下視野背景亮度過高,掩蓋光波干涉產生的暗條紋圖案,則無法進行相襯觀察。當直射參考光的亮度削減至入射前的1/9時,其亮度與衍射光亮接近,相干疊加后圖像對比度較為理想。
實驗觀察的細胞樣品中,培養基液面深度通常都大于細胞和細胞團塊厚度。細胞和培養基的折射率約為1.33-1.38,無論是透射光或衍射光,穿透液面時,因折射造成出射界面位點偏移入射方向而出現透射光傳播方向的偏移。而偏移程度與樣品層的折射率、樣品層厚度相關。發自環形光闌經透鏡聚焦形成的X型傾斜光,疊加折射所致光路偏移后,光傳播方向更分散、不規則和難以有效約束[1] 。因此,倒置相差顯微鏡下所謂的“直射光”,盡管透射光束主體走向比較集中,大部分光將從相位板共軛區經過,但必有少量“直射光”因傳播方向偏移較大,逃離共軛光環區而進入相位板補充區。
因此,有一種比較流行的說法是,光暈是因樣品中衍射光和直射衍射光在相位板的共軛區與補償區結合部竄擾污染所致。
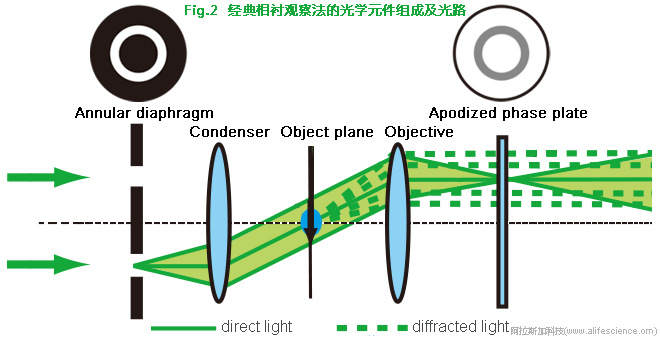
當逃逸的“直射光”從相位板補償區無損穿過時,其振幅與相位均無變化,鏡下視野的背景亮度上升,使得直射參考光(即Direct Light,下同)與衍射光(Diffracted light)相干疊加圖像中明亮條紋亮度進一步增加、面積擴大,而灰暗條紋色澤變淺。最終結果是圖像的亮度分布失衡加劇,對比度下降。而削弱穿透相位板補償區的“直射光”光量,則可降低圖像整體亮度和光暈條帶擴大化污染效應,有利于提升圖像對比度。
另一方面,若原本存在相位后延1/4波長的衍射光“誤入”共軛區,則這部分衍射光的相位會被提前1/4波長后,相當于用少量照明光經共軛區給圖像補光。而正常通行的直射參考光的相位因相位環調制而提前1/4波長。理論上,錯位衍射光與直射參考光因存在1/4波長相位差而發生相干疊,造成圖像局部參考光振幅減弱后,鏡下視野灰暗條紋振幅削弱,同樣有損暗條紋圖像的暗色。但因其光量少,對圖像整體亮度分布干擾作用遠不如“直射光”串擾效應顯著。
由此可見,直射光因亮度高,其竄擾污染對相襯圖像對比影響更大。而要降低圖像亮度,削弱光暈、增強圖像對比度,對直射光竄擾污染的治理是關鍵。
二、相位體尺寸依賴性夫瑯禾費衍射條紋分布原理
2.1 由夫瑯禾費衍射(Fraunhofer Diffraction)原理得出的推論
有道是:物理的盡頭是數學。早就有先賢數學語言對波動光學中的衍射條紋分布規律做了淋漓盡致地表述。
假設兩列傳播方向分別為A1P、A1P的子波,在P點相遇。子波從A1、A2到P點的光程r1、r2和波長決定了兩列子波此時各自的相位:
φ1 = 2π?r1 /λ , φ2 = 2π?r2 /λ ??????????????????????????????(1)
P點的相位差Δφ為:
△φ = 2π?(r1 – r2)/λ ??????????????????????????????(2)
根據惠更斯-菲涅耳原理(Huygens–Fresnel principle),從同一波陣面上發出的子波經A1、A2,在P點相遇并發生干涉時,疊加波復合振幅A的大小由二者在P點的相位差決定。A與△φ之間的聯系可用以下公式表示:
A2 = A12 + A22 + 2A1?A2?cos(φ1 -φ2) ??????????????????????????????(3)
當在P點的相位差φ1 -φ2為子波的1/2波長時,將發生相消干涉,復合振幅A最小,P點為暗斑。
當r1 – r2 =±Kλ(K=0,1,2,3,……)時,△φ=φ1 -φ2=π,復合振幅A最大,P點為量斑。
因透射傳播方向的無序性,衍射-直射光參考隨P點位置改變而相位差具有多樣性,故在像平面相干疊加形成的是明暗交織的圖像。
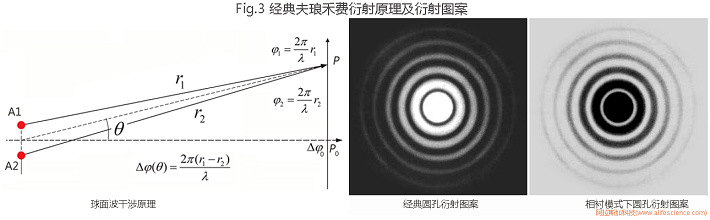
在經典夫瑯禾費衍射(Fraunhofer Diffraction)過程中,來自無限遠處平行光(如倒置相差顯微鏡中,安裝在透鏡焦點上的點光源在透鏡像方產生的平行光)通過光學圓孔(或光學狹縫,為方便表述,統一圓孔為例),并經透鏡聚焦后可在像屏上形成明暗相間的同心圓環圖案。圖案中央為衍射圓斑(艾里斑,Airy Disk),亮度最高。中心亮斑往外,為暗環-明環-暗環的交替分布。
圓孔衍射中的圓孔直徑a、衍射角θ、衍射光波長λ之間的關系可表示為:
Sinθ = ±λ/a ??????????????????????????????(4)
單色光發生圓孔衍射時,圓孔直徑大,則衍射角小。圓孔小,則光衍射角大。
衍射像面上相鄰兩個調明暗條紋中心的距離用△x表示。△x隨衍射角和物鏡焦距的增加而加大。
當θ較小時,sinθ ≈ θ,故為方便計算,中心暗斑(P0級暗斑)和相鄰的第一級亮環(稱為P1級亮環或P1級亮環)之間的△x、衍射角θ、圓孔直徑a和物鏡焦距f之間計算關系為:
△x = f?θ ??????????????????????????????(5)
此外,還可將△x與衍射光波長、圓孔直徑a、物鏡焦距f之間計算關系表述為:
△x = f?λ/a ??????????????????????????????(6)
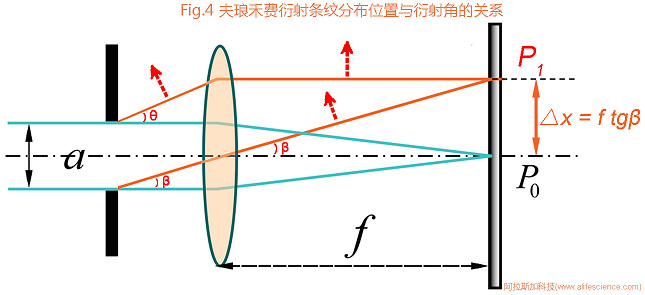
可見,是照明光波長λ、衍射角θ、衍射圓孔直徑a和物鏡焦距f這四個因素的共同作用,決定了圓孔衍射圖像的布局。而其中,照明光波長λ、衍射角θ發揮著關鍵調控作用。
實際上,所有衍射條紋,是由衍射角在0<θ<90范圍衍射光形成的多個寬窄不同的小衍射條紋相互重疊組合而成的。只是因不同單色光衍射條紋距離太近,肉眼可感知到的并非彩虹布局的條紋,而是由多色小條紋疊加形成的白色復合大條紋(將衍射像屏移到足夠遠的距離,衍射條紋圖像放大尺度足夠后,即可觀察到內向外、波長由短至長、排列有序的彩色條紋圖案)。
白光中的紅黃綠光波長長,藍紫色光波長較短。據公式(4)可知,當圓孔直徑相同時,紅黃綠光衍射角大,藍紫光衍射角小。在同一個條紋中,紅黃綠光的衍射小條紋距離P0點比短波長藍紫色條紋要遠。而小角度藍紫衍射光的條紋分布位置靠近中心點P0,具有向心分布的特點。因此,衍射條紋中波長、衍射角度光線組成的變化,會使亮色大復合條紋的幾何寬度及條紋亮度中心位置發生向心或離心方向的偏移。
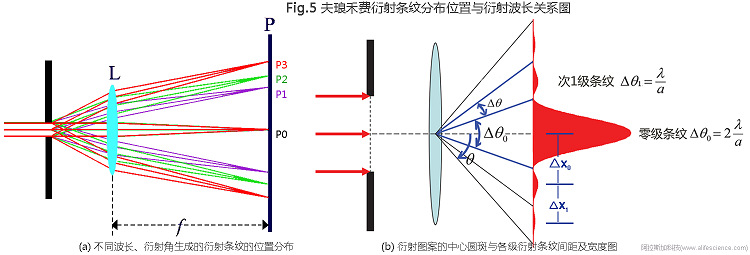
光的波長長,則亮衍射條紋角半徑大,條紋變得粗大,亮度比較分散,與相鄰條紋中心的間距大。而波長短,則衍射條紋細,條紋光能量分布集中,相鄰條紋間距縮小,從而對暗條紋分布空間擠占更明顯,使得暗條紋變窄。故白光衍射條紋寬度大于由紅黃綠等單色光形成的衍射條紋寬度,且相鄰明暗條紋間隔更小、界限更模糊。
而公式(6)則表明,相同衍射波長條件下,大圓孔衍射產生的條紋窄,光亮度分布集中,相鄰條紋,特別是明暗條紋間間距小,亮紋對暗紋分布干擾大。小圓孔衍射的條紋寬度大、條紋中心的間距大,光亮度集中程度降低,明暗條紋間的界限相對清晰,明紋對暗紋侵蝕干擾小。
2.2 用夫瑯禾費衍射原理對細胞相差觀察法光暈現象的分析
組織細胞、iPS細胞團塊、3D細胞球、類器官等透明樣品皆為微米尺度的相位體,在透射光照射會發生360°全方位衍射。故采用無限遠光學系統的倒置相差顯微鏡生成相襯圖像,可用夫瑯禾費圓孔或狹縫衍射原理來解釋[3] 。
經典瑯禾費衍射重點關注的是相干波因光程差異所致的相位差和圖像亮紋的分布。而倒置相差顯微鏡中,直射參考光、衍射光在離開相位板時就已存在1/2波長的初始相位差。因此,在相差觀察模式下的衍射模型圖中,P0并非大亮斑而是尺寸大小與明環接近的暗斑,P1級圓環則是最亮、最寬的明環。從原理上講,相位板后光路衍射圖與經典夫瑯禾費衍射圖是互為反相、黑白對調關系。
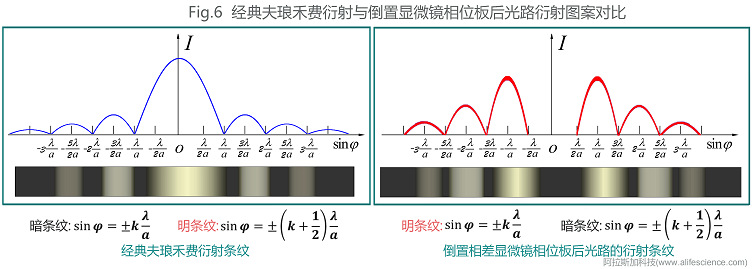
將細胞及類器官等細胞團視為大直徑衍射圓孔,則細胞器等可看作小直徑圓孔。因此,高倍鏡下的細胞相差圖像,其實是大圓孔內套小圓孔兩種尺寸衍射條紋疊加的結果。與經典瑯禾費衍射觀察重心不同,細胞圖像關注重點,并非圖案中的明環,而恰恰正是圖案中心P0級暗斑。
細胞或細胞團的直徑大,P0級衍射暗斑直徑本來就小,而緊緊環繞其周圍的是P1級明環。從圖像上看,幾乎所有細胞外緣都被亮色光環籠罩。這是因為P1級圓環光亮度極高而分布集中,與中心暗斑間距小,P1對P0“補光”,造成亮環侵蝕暗斑嚴重,掩蓋了暗斑外緣灰暗輪廓。
光暈并不局限于細胞外緣,同樣還環繞在亞細胞器周圍。在高倍鏡下可見白光沖斥細胞器間隙。只是小圓孔衍射中的P1級明環面積大而亮度較低,且與P0中心暗斑相距較遠,所以鏡下還可以大致辨清細胞器分布位置。
細胞外圍的光暈遮掩了細胞外緣輪廓,干擾了對細胞團的準確分割、細胞的計數和細胞形態測量分析。而細胞器外圍的光暈造成細胞器結構和界限難以辨識。
衍射圖案中明暗條紋的寬度(即光斑直徑或圓環寬度)、間距和亮度,是由圓孔直徑和入射光條件決定的。因衍射圓孔直徑無法選擇,要克服光暈的不利影響,只能對照明光亮度、入射波長和衍射光衍射角進行調整。
1)適度削弱透射光強度,如引入透射光中性密度濾光片(即ND濾光片,可參考《細胞圖像采集中倒置顯微鏡的透射濾光片合理使用》)下調視野整體亮度,從而降低P1級明環光量,一定程度上有助于減輕光暈。
2)配置暖色調LED透射光源,降低光源色溫。這樣既增加了入射光的波長λ,又增大了光衍射角θ,有利于拉開條紋間距,減輕高亮度條帶對相鄰暗條紋的干擾。
3)當調整光源照明條件并不適用時,則調整相位板光衍射角度成為抑制光暈的必然途徑。
無論大小圓孔衍射,復合光源照明下,P1級明環中短波長、小角度光衍射條帶的近心偏移分布,是造成明暗環帶靠近重疊的根源。剔除或削弱小角度衍射光而保留大角度衍射光,則暗斑與次級明環間距拉大,減少明暗干擾,還可使視野中心的亮度得到抑制。這或許正是Nikon公司開發的APC相差對比技術的工作原理及靈感之源。















